Andra produkter
Equilis Te
Aktiv ingrediens
ATC-kod
Djurslag
Häst.
Indikationer
Aktiv immunisering av hästar från sex månaders ålder mot tetanus för att förebygga mortalitet.
|
Immunitetens insättande: |
2 veckor efter grundvaccinationen. |
|
Immunitetens varaktighet: |
17 månader efter grundvaccinationen. |
|
2 år efter första revaccinationen. |
Dos och administreringssätt
Intramuskulär användning.
Låt vaccinet anta rumstemperatur före användning.
Vaccinationsschema:
Grundvaccination
En dos (1 ml) ges som en intramuskulär injektion enligt följande schema:
• Grundvaccination: Den första injektionen ges från sex månaders ålder, den andra injektionen ges fyra veckor senare.
Revaccination
Den första revaccinationen ska inte ges senare än 17 månader efter grundvaccinationen. Därefter rekommenderas ett maximalt intervall av två år (se schema).
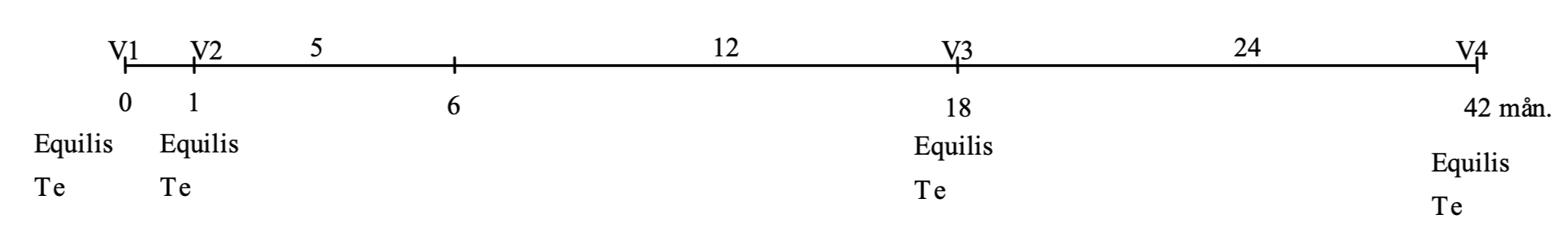
Vid ökad infektionsrisk eller otillräckligt intag av råmjölk kan ytterligare en initial injektion ges vid fyra månaders ålder som sedan åtföljs av det fullständiga vaccinationsprogrammet (grundvaccination vid sex månaders ålder och fyra veckor senare).
Samtidig aktiv och passiv immunisering (nödvaccination)
Vaccinet kan ges tillsammans med Tetanus Serum för behandling av skadade hästar som inte blivit immuniserade mot tetanus. I sådana fall kan den första vaccindosen (V1) i grundvaccinationen ges samtidigt med den profylaktiska dosen av Tetanus Serum. Separata injektionsställen och användning av separata sprutor och kanyler ska användas. Detta ger ett passivt skydd mot tetanus under minst 21 dagar efter samtidig administrering. Den andra vaccindosen (V2) bör ges fyra veckor senare. En tredje vaccination med Equilis Te bör ges åtminstone fyra veckor senare. Samtidig administrering med Equilis Te och Tetanus Serum från Intervet kan reducera aktiv immunitet mot tetanus jämfört med om endast Equilis Te används i frånvaro av tetanusantitoxinserum.
Biverkningar
Häst:
|
Sällsynta (1 till 10 av 10 000 behandlade djur): |
Svullnad vid injektionsstället1, smärta vid injektionsstället2. |
|
Mycket sällsynta (färre än 1 av 10 000 behandlade djur, enstaka rapporterade händelser inkluderade): |
Feber3, letargi3, aptitlöshet3, överkänslighetsreaktion4. |
1 En diffus, hård eller mjuk svullnad (max 5 cm i diameter) som avklingar inom två dagar. I mycket sällsynta fall kan en lokal reaktion som är större än 5 cm och som eventuellt kvarstår i mer än två dagar förekomma.
2 Smärta vid injektionsstället kan ge upphov till övergående funktionsobehag (stelhet).
3 Feber som ibland åtföljs av letargi och aptitlöshet kan förekomma under en dag och i undantagsfall kvarstå upp till tre dagar.
4 Inkluderar anafylaxi (ibland livshotande). Om sådan reaktion uppstår ska lämplig behandling ges utan fördröjning.
Det är viktigt att rapportera biverkningar. Det möjliggör fortlöpande säkerhetsövervakning av ett läkemedel. Rapporter ska, företrädesvis via en veterinär, skickas till antingen innehavaren av godkännande för försäljning eller till den nationella behöriga myndigheten via det nationella rapporteringssystemet. Se bipacksedeln för respektive kontaktuppgifter.
Utlämning
Receptbelagt| PRIS | Priset är endast synligt för yrkesverksamma. Skapa din gratis profil på VETiSearch idag.. Logga in |
|---|---|
| VNR | 061343 |
| GTIN | • • • • • • • • • 3430 |

 VERIFIERADE DATA
VERIFIERADE DATA













